アルミニウムイオン(Al3+)にNaOHを加えたときの反応については、以前に検討しました(2019/04/14)。今回は、Al3+にアンモニア水を加えた場合についてエクセルのソルバー機能を用いて定量的に解析します。
具体的には、濃度Cal mol/Lの硝酸アルミニウム溶液に、濃度がCnh mol/Lとなるようにアンモニアを添加することを考えます。計算の煩雑さを避けるため、アンモニアの添加による溶液の体積変化は無視します。
また、Al(OH)3の溶解度積をpKsp = 32.3
アンモニウムイオンの酸解離定数をpKn = 9.37
アルミニウムのヒドロキソ錯体の生成定数を、
logβo1=9.0, logβo2=17.9, logβo3=25.2, logβo4=33.3
とし、これ以外の平衡は無視します。活量係数は1とします(25℃)。
Cal = 0.1 mol/Lとし、Cnhの値を変化させたときのAl(OH)3の溶解度Sおよび化学種濃度をエクセルのソルバー機能を用いて求めます。
●ソルバーのパラメータ設定
・目的セル:電荷バランス、Q =0
・変数セル:pH およびpNH3
・制約条件:アンモニアの物質バランス、R = Cnh-[NH3’] = 0
●特に、沈殿の生成・消滅境界におけるパラメータ設定は、
・目的セル:電荷バランスQ =0
・変数セル:pH, pNH3 およびCnh
・制約条件:R = 0 および[Al][OH]^3/Ksp = 1
●[Al]の計算式
・沈殿のないとき:[Al] =Cal/α
・沈殿のあるとき:[Al] =Ksp/[OH]^3
結果は次の通りです。
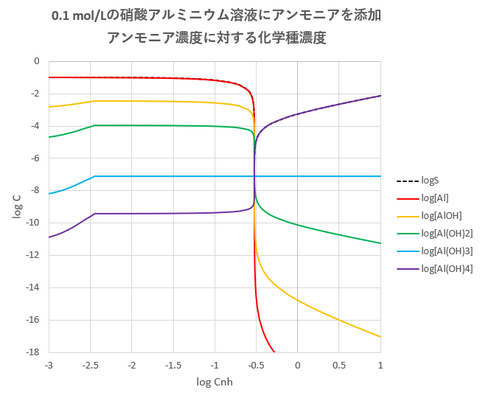
図-1(アンモニア濃度に対する溶解度・化学種濃度)
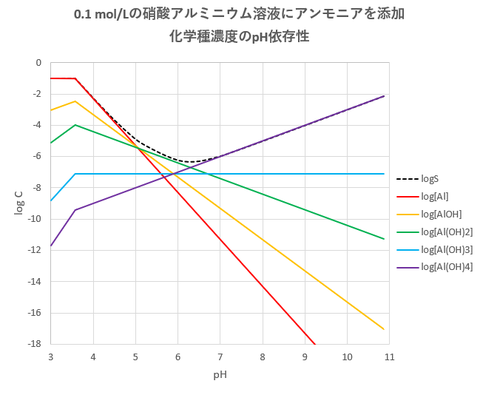
図-2(溶解度・化学種濃度のpH依存性)
図-3(溶解度および沈殿率)
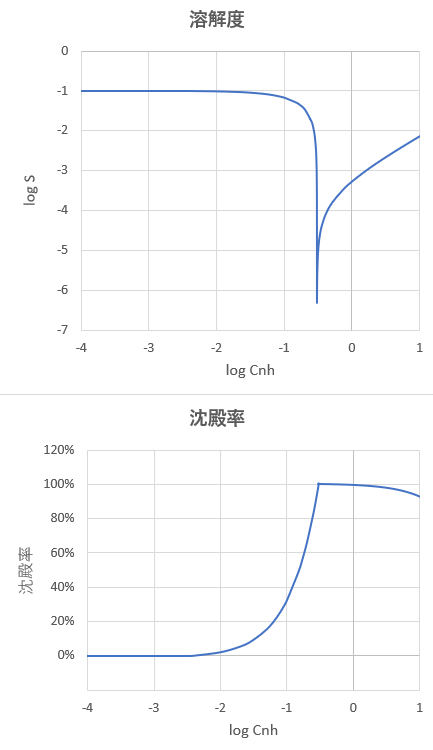
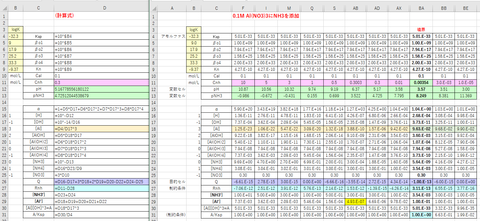
図-4(エクセルシート(計算式の例))
0.1 mol/L硝酸アルミニウムにアンモニアを加えると、添加したアンモニア濃度が0.004 mol/L (pH3.6)付近でAl(OH)3の沈殿生成が始まり、当量点(Cnh=0.3mol/L) (pH6.4)付近で溶解度は最小(S=4.9×10^-7 mol/L)となります。さらにアンモニアを過剰に加えると、溶解度が増加することが分かります。
アルミニウムの化学種について言うと、当量点(Cnh=0.3 mol/L)付近まではAl^3+ が主成分ですが、当量点を過ぎるとAl(OH)4^-が優勢となります。
コメント