第1属を除いた塩酸酸性溶液に硫化水素ガス(H2S)を通じると硫化物が沈殿するイオンは第2属に分類されます。このうち多硫化ナトリウムに溶解しないものは<第2属A>(Pb(II), Bi(III), Cu(II), Cd()II))、溶解するものは<第2属B>(Hg(II), As(III, V), Sb(III, V), Sn(II, IV))に区分されます。
今回は、第2属の分属および第2属Aの分離・確認操作について考えます。
<<第2属の分属および第2属Aの分離・確認操作>>
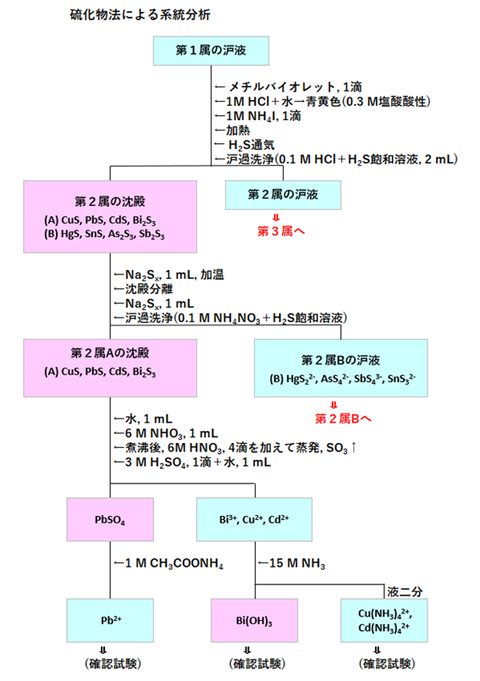
第2属の分属および第2属Aの分離操作のフローチャートを図-1に示し、第2属Aの確認操作の概要を図-2に示します。Pb2+は大部分が第1属として処理されますが、PbCl2の溶解度は比較的大きいので一部が第2属に来ます。
<<第2属の分属操作>>
<硫化物の溶解度と酸濃度の関係>
多くのイオンが硫化物イオン(S2-)と反応して硫化物沈殿を生成しますが、酸濃度を調整すると特定イオンのみが沈殿します。酸濃度と硫化物の溶解度の関係についてはすでに詳しく説明したので(2019-12-22)、ここではキーポイントのみを示します。
硫化水素は2価の弱酸で、次のように解離します。
H2S ⇄ H+ + HS-
HS- ⇄ H+ + S2-
酸解離定数は、常温において、
K1 = [H][HS]/[H2S] ,
pK1≒7.0
K2 = [H][S]/[HS] , pK2≒14.0
K1K2 = [H]^2[S]/[H2S]
硫化水素ガスを飽和させた溶液中の水和硫化水素分子(H2S)の濃度はpHにかかわりなく一定で、常温常圧で[H2S]≒0.1 mol/Lです。
また、硫化物イオン(S2-)は様々な金属イオンと難溶性の硫化物を生成します。
2M+ + S2- ⇄ M2S
M2+ + S2- ⇄ MS
2M3+ + 3S2- ⇄ M2S3
沈殿が生成して溶解平衡が成立するとき溶解度積は、
M+に対して、Ksp = [M]^2[S]
M2+に対して、Ksp = [M][S]
M3+に対して、Ksp = [M]^2[S]^3
となります。
以上の関係から、他の副反応等がないと仮定すると、硫化物の溶解度(s)と水素イオン濃度の関係は、s=[M], [S] = K1K2[H2S]/[H]^2なので、
M+に対して、
s = [M] = √(Ksp/[S]) = √{Ksp[H]^2/(K1K2[H2S])}
M2+に対して、
s = [M] = Ksp/[S] = Ksp[H]^2/(K1K2[H2S])
M3+に対して、
s = [M] = √(Ksp/[S]^3) = √{Ksp([H]^2/(K1K2[H2S]))3}
したがって、硫化水素ガスを溶液に通じて飽和させた溶液中([H2S]=0.1 mol/L)ではK1K2[H2S]=10^-22なので、硫化物の溶解度は、
M+に対して、s = 10^11×[H]×√(Ksp)
M2+に対して、s = 10^22×[H]^2×Ksp
M3+に対して、s = 10^33×[H]^3×√(Ksp)
となります。
Ksp既知のイオンについてpHと溶解度の関係を図-3に示します。
図-3
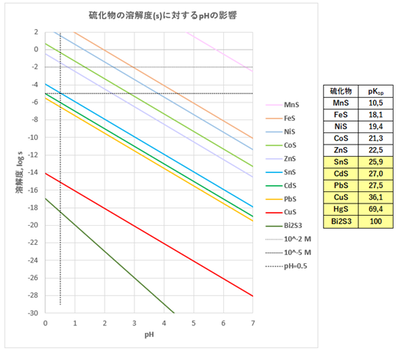
(データはA. E. Martell and R. M. Smith,
"Critical Stability Constans, vol. 4 "(1976)より)
<第2属の硫化物沈殿>
0.01 mol/Lの金属イオンについて、溶解度が10^-5 mol/L以下ならば定量的に沈殿する(99.9%以上)と考えることにすると、図-3から、0.3
mol/L HCl酸性溶液(pH=0.5)において硫化水素ガス(H2S)を通じると、Mn(II), Fe(II), Ni(II), Co(II), Zn(II)は沈殿せず、Sn(II),
Cd(II), Pb(II), Sb(III), Cu(II), Bi(III), Hg(II)は沈殿することが(他の副反応等は無視して)大枠として読み取れます。
Sb(III), Sn(VI)も定量的に沈殿します。ヒ素についてはNH4Iを加えてAs(V)をAs(III)に還元することにより定量的に沈殿します。
このように塩酸酸性溶液([HCl]=0.3 mol/L)でH2Sを通じると硫化物を沈殿するイオンが第2属に分類されます(*1)。沈殿の色はCdS(黄), PbS(黒), CuS(黒), HgS(黒),
SnS(褐), SnS2(黄), Sb2S3(赤橙), As2S3(黄), Bi2S3(褐)です。第2属の硫化物沈殿を沪過した沪液は第3属へ行きます。
(*1) なぜ[HCl]=0.3 mol/Lとしたかの理由の一つとして、Cl-濃度が高すぎると金属の塩化物錯体が生成して溶解度が高くなることがあげられる。たとえば、CdSの場合、[HCl]=0.3 mol/Lを超えると沈殿は不完全になる(2021-08-05)。
<<第2属Aの分離・確認>>
<多硫化ナトリウムによる分離>
Na2S+NaOHの水溶液にイオウ(S)を溶解すると種々のn値(n=2~5)を持つ混合物(多硫化ナトリウム, Na2Sn)が得られます。この多硫化ナトリウムを第2属沈殿に加えるとBi2S3, CuS, PbS, CdS(第2属A)は沈殿のままですが、HgS, As2S3,
Sb2S3, SnS, SnS2(第2属B)はチオ錯イオンを作って溶解します(*2)。このときAs(III), Sb(III),
Sn(II)はそれぞれAs(V), Sb(V), Sn(IV)に酸化されます。
HgS + Sn2- ⇄
HgS22- + (n-1)S
As2S3 + 3Sn2-
⇄ 2AsS42- + (3n-5)S
Sb2S3 + 3Sn2- ⇄ 2SbS42-
+ (3n-5)S
SnS + Sn2- ⇄ SnS32- + (n-2)S
SnS2 + Sn2- ⇄ SnS32- + (n-1)S
このあと沪過洗浄すると、沪液は第2属Bに行き、沈殿(Bi2S3,
CuS, PbS, CdS)は第2属Aとして残ります。NH4NO3の添加は沈殿の解膠(コロイド化)を防ぐためです。
(*2) もし多硫化アンモニウムを用いるとHgSは溶解せず、第2属Aになる。
<第2属A沈殿の溶液化>
第2属Aの沈殿は硝酸を加えて煮沸して溶液化し、さらに硝酸を加えSO3の白煙がでるまで蒸発します。この操作により第2属Aの硫化物沈殿は酸化されて、溶解します(Pb2+, Bi3+,
Cu2+, Cd2+)。
<<Pb2+の分離と確認>>
<H2SO4による沈殿分離>
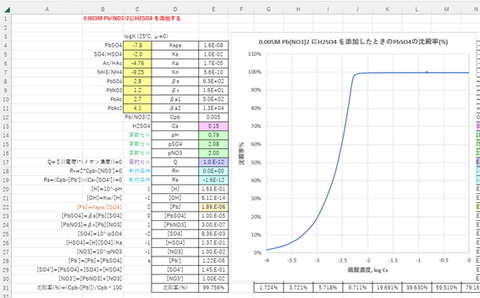
前項の第2属Aイオンを含む溶液にH2SO4を加えるとPb2+だけがPbSO4の沈殿を作ります。沪過後沈殿に酢酸アンモニウム(NH4Ac)を加えるとPbSO4沈殿はPb(Ac)2錯体を作って溶解します。この様子をエクセルで計算します。
PbCl2の溶解度から考えて第1属から第2属に流れてくるPb2+の量は、溶液1mLあたり0.005 mmol程度と考えられます。0.005 mol/LのPb(NO3)2溶液にH2SO4を加えたときのH2SO4濃度と沈殿率の関係を図-4に示します。
<酢酸ナトリウムによる溶解>
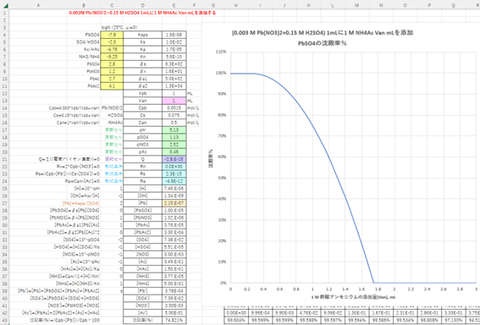
PbSO4 0.005 mmolを含む溶液1 mLに1 mol/L酢酸アンモニウム溶液を加えたとき、酢酸アンモニウム溶液の添加量と沈殿率の関係について求めました。計算結果を図-5に示します。PbSO4
0.005 mmolを含む溶液1 mLにおよそ1.8 mL以上の1 mol/L酢酸アンモニウム溶液を加えるとPbSO4沈殿が消滅して溶液化する結果となりました。
<Pb2+の確認>
Pb2+の確認は第1属での場合と同様、ベンジジン試薬、K2CrO4によって行います(2022-12-25)。

コメント